Antibiotici e antibiotico resistenza
L’antibiotico resistenza è una delle conseguenze dell’utilizzo non regolamentato dei farmaci antibiotici.
Gli antibiotici hanno trasformato in modo radicale la gestione e il trattamento delle infezioni batteriche. Hanno salvato milioni di vite diventando uno strumento terapeutico indiscusso.
Molti decenni dopo la loro introduzione però, a causa della crescente diffusione di microrganismi resistenti e multi-resistenti, il dibattito sul loro utilizzo si è riacceso prepotentemente e le infezioni batteriche sono diventate nuovamente una seria minaccia.
In particolare, lo sviluppo di ceppi multiresistenti (MDR), resistenti cioè a tre o più classi di antimicrobici, o di ceppi ampiamente resistenti ai farmaci (XDR), resistenti cioè a tutte tranne una o due classi di antimicrobici, è motivo di grande preoccupazione.
Negli ultimi 10 anni, la mancanza di nuovi antibiotici per combattere l’insorgenza di MDR, XDR e batteri resistenti ad ogni antibiotico (PDR) è stata la principale preoccupazione delle agenzie sanitarie nazionali e internazionali. Sebbene nuove molecole siano state recentemente approvate, pochissimi sono gli antimicrobici che sono stati sviluppati per combattere i batteri MDR.
Negli ultimi 10 anni, la mancanza di nuovi #antibiotici per combattere l’insorgenza di MDR, XDR e PDR è stata la principale preoccupazione delle agenzie sanitarie nazionali e internazionali | #AntibioticoResistenza #ECM #MMG Share on XL’antibiotico resistenza in Italia e nel mondo
La resistenza agli antibiotici è un grave problema in tutte le parti del mondo. Dai dati forniti dall’OMS (Organizzazione Mondiale della Sanità) ogni anno muoiono nel mondo 700.000 persone a causa di un’infezione causata da batteri resistenti alla terapia antibiotica.
Di queste, 33.000 sono registrate in Europa e 10.000 riguardano l’Italia. Nel nostro paese esistono sistemi di sorveglianza coordinati dall’Istituto Superiore di Sanità:
- il Sistema di Sorveglianza nazionale dell’antibiotico-resistenza
- il Sistema di Sorveglianza delle CPE (batteriemie da enterobatteri produttori di carbapenemasi, una classe di antibiotici ad ampio spettro)
a loro volta collegati al sistema europeo EARS-Net (European Antimicrobial Resistance Surveillance Network) che raccoglie i dati a livello europeo nel Surveillance Atlas of Infctious Diseases.
Nel 2018 il sistema di sorveglianza ha registrato nel nostro paese percentuali di resistenza, delle 8 principali specie batteriche responsabili di gravi infezioni nosocomiali, più alte rispetto alla media europea.
L'#AntibioticoResistenza è un grave problema in tutte le parti del mondo. I dati OMS rilevano che ogni anno muoiono nel mondo 700.000 persone a causa di infezioni causate da batteri resistenti | #ECM #MMG Share on XPer approfondire le cifre del consumo degli antibiotici in Italia si consiglia di consultare il Rapporto Nazione AIFA del 2018.
Antibiotico resistenza in Europa
In Europa, la rete europea di sorveglianza della resistenza antimicrobica (EARS-Net) ha fornito dati di riferimento sulla resistenza antimicrobica a partire dal 1999. Negli ultimi anni è aumentata la proporzione di K. pneumoniae ed E. coli con resistenza ai fluorochinoloni, cefalosporine di terza generazione, aminoglicosidi e resistenza combinata a tutti e tre i gruppi antibiotici.
Lo stesso dicasi per quanto riguarda Acinetobacter spp. la cui percentuale di isolati resistenti è aumentata in particolare nel sud e sud-est del continente europeo. Dati simili sono stati osservati per Staphylococcus aureus meticillino-resistente (MRSA) che ha evidenziato livelli di resistenza variabili tra lo 0.9 e il 56% a seconda del paese.
Classificazione internazionale dei germi multiresistenti
Un gruppo di esperti internazionali riuniti per un’iniziativa congiunta tra l’ECDC e il CDC, è stato incaricato di creare una terminologia internazionale standardizzata per descrivere i profili di resistenza acquisiti in organismi multiresistenti.
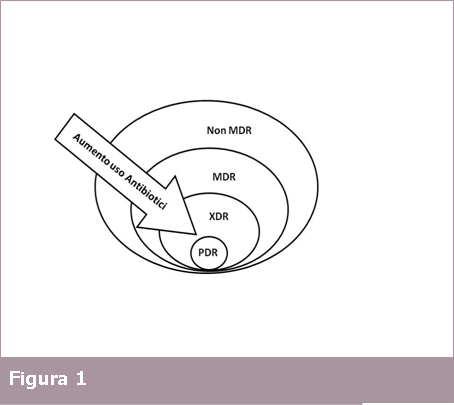
I germi multiresistenti sono stati quindi suddivisi in tre categorie a seconda del loro profilo di resistenza:
- MDR: non suscettibili ad almeno 1 agente in 3 categorie antimicrobiche;
- XDR: organismi ampiamente resistenti ai farmaci – non suscettibili ad almeno 1 agente in tutte le categorie antimicrobiche tranne due o meno;
- PDR: organismi non suscettibili a nessuno degli agenti in tutte le categorie antimicrobiche.
Negli ultimi anni è stata lanciata una nuova raccomandazione sulla classificazione delle infezioni causata da patogeni Gram-negativi e Gram-negativi multiresistenti coniando l’acronimo “ESCAPE” (E. faecium, S. aureus, C. difficile, A. baumannii, P. aeruginosa e Enterobacteriaceae spp.) al fine di ricordare meglio i germi più pericolosi e frequenti.
I germi multiresistenti sono suddivisi in tre categorie a seconda del loro profilo di resistenza: MDR, XDR, PDR | #AntibioticoResistenza #ECM #MMG Share on XLa resistenza nei germi Gram-positivi
I germi gram-positivi MDR sono tra i principali patogeni umani. Tra questi, Staphylococcus aureus meticillino-resistente (MRSA), Enterococcus faecium resistente alla vancomicina (VRE) e Streptococco resistente sono stati designati come gravi minacce pubbliche dal CDC.
Infatti, MRSA e VRE sono le principali cause di infezioni associate all’assistenza sanitaria negli Stati Uniti. Stime prudenti suggeriscono che essi causino più di 12.000 decessi all’anno. Allo stesso modo, le infezioni dovute a S. Pneumoniae farmaco-resistente, la principale causa di polmonite batterica e meningite negli adulti, sono stimate causare oltre 19.000 ammissioni in ospedale e 7000 morti all’anno nei soli Stati Uniti.
Le basi genetiche e biochimiche della resistenza antimicrobica nei batteri gram-positivi sono diverse e spesso si differenziano tra generi e/o specie.
La resistenza nei germi Gram-negativi
I meccanismi di resistenza più comuni dei batteri Gram-negativi, includono la produzione di vari enzimi inattivanti e la diminuzione dell’ingresso degli agenti antimicrobici all'interno del micro-organismo | #AntibioticoResistenza Share on XI meccanismi coinvolti nello sviluppo della resistenza antimicrobica nei Gram-negativi possono essere intrinseci, acquisiti o adattivi:
- la resistenza intrinseca deriva dalle caratteristiche di un particolare microorganismo, come il possesso di una membrana esterna a bassa permeabilità e pompe di efflusso in grado escludere particolari agenti antimicrobici.
- la resistenza acquisita deriva dall’incorporazione di nuovo materiale genetico come plasmidi, trasposoni, integroni e DNA nudo da parte di germi originariamente sensibili agli agenti antimicrobici.
- i processi della resistenza adattiva implicano un aumento della capacità dei batteri di resistere all’attività antimicrobica. Questo è il risultato di alterazioni nell’espressione genica e/o proteica a causa di una precedente esposizione a un trigger ambientale o a concentrazioni sub-inibitorie di farmaci antimicrobici. Possono essere mediati da plasmidi o da cromosomi il cui posizionamento su elementi genici trasferibili ne facilita la diffusione a batteri della stessa specie o specie diverse.
I meccanismi di resistenza più comuni caratterizzanti i batteri Gram-negativi, includono la produzione di vari enzimi inattivanti, la diminuzione dell’ingresso degli agenti antimicrobici all’interno del micro-organismo a causa di una riduzione del numero di canali di ingresso delle proteine (porine) che facilitano il loro assorbimento e l’aumento dell’espulsione dell’agente antimicrobico dal germe a causa di una maggiore espressione di pompe di efflusso citoplasmatico.
Fattori di rischio per l’infezione da Gram-negativi MDR
I dati attualmente disponibili suggeriscono che la prevalenza dei batteri Gram-negativi MDR sia in aumento in tutto il mondo. Numerosi fattori di rischio possono aumentare la probabilità di infezione da parte di questi microorganismi:
- precedente terapia antimicrobica, in particolare con un agente ad ampio spettro, nei precedenti 90 giorni;
- durata del ricovero per 5 giorni;
- alta prevalenza di organismi resistenti in ambiente ospedaliero;
- terapia immunosoppressiva;
- altri fattori, tipo una degenza in ospedale per 2 giorni nei precedenti 90, la residenza in una casa di riposo, dialisi cronica, presenza di ferite a lenta guarigione, diabete, terapie per infusione endovenosa.
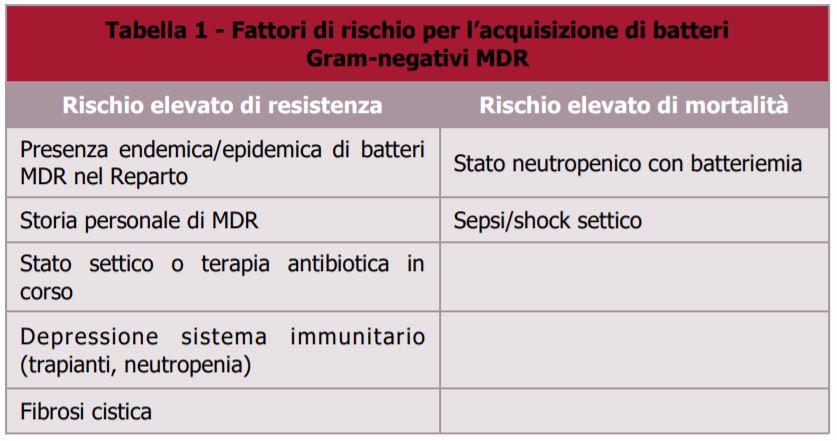
Inoltre, non possono non essere menzionati altri fattori che hanno contribuito alla persistenza e alla diffusione dei batteri gram-negativi MDR:
- l’uso eccessivo di agenti antimicrobici nella comunità che ha portato allo sviluppo di meccanismi di resistenza adattiva da parte dei batteri;
- la cattiva gestione dei farmaci antibiotici per cui l’uso di più agenti ad ampio spettro ha contribuito a perpetuare il ciclo di resistenza;
- la mancata adozione di buone pratiche per il controllo delle infezioni;
- la carenza di nuovi agenti antimicrobici specifici.
Uso non regolamentato dei farmaci antibiotici: un problema sottovalutato
Infine, l’uso non regolamentato di farmaci antibiotici in medicina veterinaria e in zootecnia ha avuto un impatto significativo sullo sviluppo della resistenza.
L’aumento dei tassi di resistenza tra i batteri gram-negativi genera naturalmente forti preoccupazioni dati i problemi oggettivi correlati alla scarsità delle opzioni terapeutiche a disposizione e il conseguente elevato tasso di mortalità tra i pazienti.
L’utilizzo non regolamentato di #antibiotici in medicina #veterinaria e in #zootecnia ha avuto un impatto significativo sullo sviluppo dell' #AntibioticoResistenza | #ECM #MMG Share on XIn aggiunta all’aumento dei tassi di mortalità, le infezioni da germi gram-negativi MDR sono anche associate a un maggiore onere economico dovuto al loro maggiore severità e maggiore utilizzo di risorse per una degenza più lunga in ospedale e/o ICU.
Antibiotico resistenza: considerazioni generali di trattamento nella pratica clinica
La crescente prevalenza di batteri gram-negativi MDR pone una seria sfida ai medici che gestiscono malati critici con infezioni acute.
In questi casi aumenta la probabilità di fallimento del trattamento iniziale con in più il rischio concreto che un uso eccessivo di farmaci antimicrobici ad ampio spettro possa avere l’effetto indesiderato di aumentare la probabilità di resistenza.
Il principio fondamentale della gestione della terapia antimicrobica in questi pazienti è la tempestività dell’inizio del trattamento antimicrobico ottimale. Idealmente, prima di iniziare la somministrazione di un antibiotico, dovrebbero essere ottenute le colture dalle sedi ritenute sede di infezione.
Il principio fondamentale della gestione della terapia antimicrobica nei pazienti con ingezioni da batteri GRAM-Negativi MDR è la tempestività dell’inizio del trattamento antimicrobico ottimale | #AntibioticoResistenza #MMG Share on XGestione iniziale dei pazienti con sospette infezioni da batteri gram-negativi
Se esiste la necessità clinica di iniziare il trattamento prima dei risultati dei test di laboratorio, le raccomandazioni per la gestione iniziale di pazienti con infezioni acute sospettate da organismi gram-negativi suggeriscono:
- considerare la malattia di base in termini di gravità e se si tratta di un tipo di infezione in cui è probabile una eziologia da batteri gram-negativi MDR;
- stabilire se il paziente ha avuto un qualsiasi tipo di colonizzazione batterica precedente il cui trattamento potrebbe aver aumentato la probabilità di organismi resistenti;
- tenere in considerazione l’epidemiologia del reparto;
- somministrazione precoce di una terapia antimicrobica empirica basata su queste considerazioni con successivo suo aggiustamento sulla base dei risultati del laboratorio microbiologico.
A seconda del microorganismo sospettato, un appropriato regime empirico può includere la combinazione di una cefalosporina ad ampio spettro o antipseudomonas più un amminoglicoside, un agente inibitore delle beta-lattamasi in combinazione con un amminoglicoside o un carbapenemico.
Una volta disponibili i risultati del laboratorio, il regime di trattamento può essere adattato e ridotto. Sebbene i regimi di antibiotico-terapia di combinazione possono comportare un aumento dei costi e degli effetti avverso dei farmaci, la logica per il loro utilizzo almeno in fase iniziale è basata sul poter utilizzare il sinergismo tra i farmaci, la prevenzione (o ritardo) della comparsa della resistenza e l’ampliamento della copertura antimicrobica quando il rischio di organismi MDR è alto utilizzando due farmaci diversi con meccanismi di azione diversi.
L’importanza di un trattamento tempestivo
Dalla scoperta della penicillina a oggi, numerosi antibiotici sono stati messi a disposizione dei clinici, ma poco dopo, senza eccezioni, sono emersi batteri resistenti.
Si tratta di un fenomeno estremamente rilevante in termini di morbidità e mortalità per i pazienti, impegno dei servizi sanitari e costi per la collettività.
Un trattamento appropriato e tempestivo con farmaci antibiotici utilizzando strategie di combinazione o nuove molecole sono la pietra angolare per il trattamento di tali casi complessi. Tuttavia, anche nel caso del ricorso a strategie e trattamenti corretti, il tasso di mortalità dei pazienti con infezioni da agenti MDR rimane più alto di quello osservati nei pazienti con sepsi da batteri no-MDR.
L' #AntibioticoResistenza è fenomeno estremamente rilevante in termini di morbidità e mortalità per i pazienti, impegno dei servizi sanitari e costi per la collettività | #ECM #MMG Share on XNegli ultimi anni, è diventato chiaro che il sistema immunitario gioca un ruolo determinante. Un’attenzione speciale dovrebbe quindi essere dedicata a questo particolare settore. Quella della resistenza antimicrobica è una sfida oramai vitale nelle ICU poiché in questi reparti si concentrano i pazienti a maggior rischio.
Pertanto, presso questi reparti esiste la precisa responsabilità di mettere in atto tutte le misure per individuare tempestivamente i fattori di rischio e i pazienti affetti o portatori di germi MDR, monitorare i livelli di resistenza e promuovere programmi di controllo delle infezioni. Una revisione delle politiche di trattamento antibiotico, specialmente in ambito ospedaliero, è obbligatoria per ridurre la pressione selettiva.
Per garantire un adeguato livello di assistenza è necessario conoscere le dimensioni del problema dell’antibiotico resistenza e coinvolgere, in un’ottica multidisciplinare e multi professionale, tutte le figure professionali ritenute utili per stabilire trattamenti efficaci e appropriati.
Sei Medico di Medicina Generale?
Iscriviti ai nostri corsi
Percorso Formativo Doctorline 36 crediti ECM
Doctorline Smart Pack – Terapia nutrizionale nel paziente nefropatico – 5 crediti ECM gratuiti
Articolo tratto dalla lezione del Percorso Formativo Doctorline del Prof. Gianni Biancofiore: “La terapia antibiotica nelle infezioni da germi multiresistenti”
CONTATTACI SUBITO e richiedi la versione integrale della Lezione 👇








Devi effettuare l'accesso per postare un commento.